
2022 年 12 月,美國眾議院通過《FDA 現代化法案 2.0》(FDA Modernization Act 2.0)一項重要法案,旨在對美國食品和藥物管理局(FDA)的某些監管流程進行現代化改革。這項法案的通過,對捍衛動物權利來說具有革命性的影響,標誌著動物實驗在藥物研發中不再是必須,推動了更人道且高效的替代技術。如器官晶片、細胞培養和電腦模擬等,顯著減少了對動物實驗的依賴。這不僅提升了藥物開發效率,也標誌著一個更人道的科學研究時代來臨,對全球動物福利產生了深遠影響。

美國食品和藥物管理局 (FDA) 作為全球食品和藥品監管的指標,因其嚴格的科學標準、公正的審批流程、推動創新技術及國際影響力,確保產品安全性、有效性,在全球市場中享有信任和權威。法案通過前,製藥公司進行臨床試驗前,必須依照規定使用動物(如老鼠、兔子或猴子)來測試藥物的安全性和有效性。這意味著動物實驗是藥物獲得批准的必要步驟,無論當時是否有先進的非動物技術,企業都無法直接跳過這個過程。
然而,這種嚴格的要求也帶來了一些挑戰。動物實驗通常需要耗費大量時間和資源,延長了藥物研發的進度,並增加了成本。一定程度上限制了製藥公司的創新和靈活性,使得他們在選擇替代技術時受到局限。平均來說,藥物開發需要12年時間,花費約24億美元,過程分為三個主要階段。首先為藥物探索,包括發現潛在藥物、評估活性與毒性,選出有價值的候選藥物進行進一步測試。下一階段為臨床前試驗,一定要在動物身上進行毒理和藥效試驗,並確保製造過程與安全性,才能進行到下一階段的人體試驗。最後為臨床試驗階段,分為四期。前三期涉及人體測試藥物的安全性、有效性及副作用,通過後申請上市並進行第四期監測。

為什麼會有動物實驗?
動物實驗的出現以及他的發展源於一系列歷史事件及科學需求,促使政府與監管機構將動物實驗納入藥物開發的標準程序。作為決策考量的關鍵原因有以下分析:
理解疾病機制:動物和人類的生理運作非常相似,通過研究動物,科學家能更好地了解疾病是如何發展的,這有助於他們找到治療方法。
測試藥物安全性:在測試藥物對人體是否安全之前,科學家需要一個可控的方式來檢測藥物是否有害。動物實驗可以在不危及人類的情況下測試新藥的毒性和副作用。
檢驗藥物有效性:除了安全性外,動物實驗也用來檢查藥物是否有效治療疾病。通過觀察動物的反應,科學家可以評估藥物是否值得進一步測試在人類身上使用。
法律與監管要求:過去發生的藥物安全問題造成大量人員傷亡,這促使許多國家規定,在進行人體試驗之前,藥物必須先經過動物測試,以保護公眾健康。
替代技術尚未成熟:當動物實驗成為標準時,科學家還沒有足夠的替代技術來取代它。動物實驗提供了完整生物體的反應,而這些反應在實驗室內的細胞或器官培養中難以複製。
關鍵性的把動物實驗列為藥品上市前的「必要」手段,是源於歷史上一些嚴重的公共健康危機和事件。1937 年的「磺胺酏劑事件」,美國麥森吉爾公司公司推出了一種含有磺胺的新藥物,主要用於治療細菌感染引發的病症。但使用了有毒的溶劑——二甘醇。該藥物未經充分測試便投入市場,導致超過 100 人死亡,其中大部分是兒童。這一悲劇直接促使美國通過了《1938 年聯邦食品、藥物和化妝品法案》,要求藥物在上市前必須進行安全性測試,最初的測試手段主要依賴動物實驗。
1950-60 年代,沙利竇邁事件(Thalidomide Scandal)。沙利竇邁被廣泛用於治療孕婦的晨吐,然而,該藥物未經充分的動物和人類試驗,數據顯示新生兒畸形的發生率與沙利竇邁的銷售量呈現一定的相關性,遂對反應停的安全性產生懷疑。在之後的毒理學研究顯示,沙利竇邁對靈長類動物有很強的致畸性。這一事件加強了對藥物的嚴格測試要求,並推動了更嚴格的藥物審批流程,包括使用動物實驗來檢測潛在的副作用。
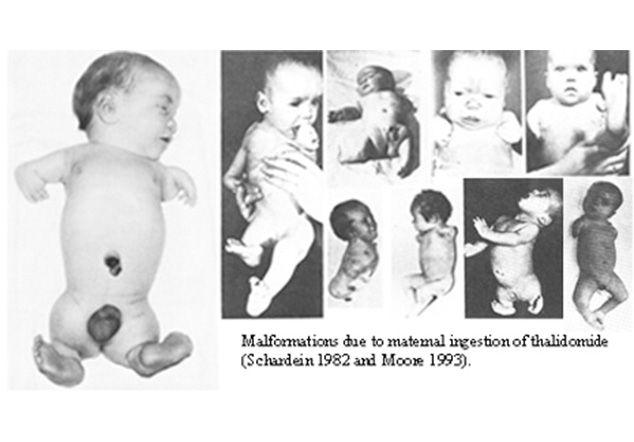
沙利竇邁事件後,美國國會通過了對《1938 年聯邦食品、藥物和化妝品法案》的修正案(Kefauver-Harris Amendment),嚴格要求製藥公司必須證明藥物的安全性和有效性,這通常需要通過動物實驗來進行評估。這項修正案為動物實驗成為標準程序奠定了法律基礎。
為了人類健康福趾與社會公共安全的發展,動物實驗在醫藥研發、生物醫學的基因研究、毒理學的化學品和環境毒性測試、食品和營養科學的食物添加劑安全性測試,以及神經疾病研究和心理學的行為研究等各方面,成為不可或缺的重要環節。
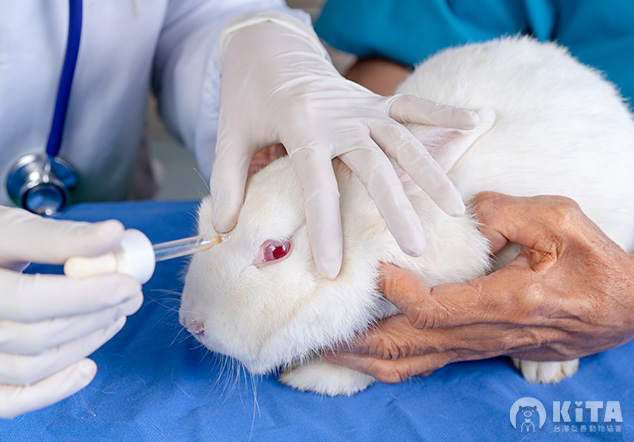
藥物開發“非”最多使用實驗動物數量的領域
根據台灣 2022 年各動物科學應用機構監督報告統計分析,實驗動物的研究計畫領域及數量分類以「醫學研究」 (4,414 件,55.73%) 最多,「藥物 (含中藥草)」 (1,245 件,15.7%) 次之。此外, Thomas Hartung 博士是美國約翰霍普金斯大學毒理學教授,也是動物實驗替代中心主任。他的文章「動物模型在藥物開發中的(誤導性)角色」中提到,1970 年代之前,許多動物如老鼠、大象、猴子等,因和人類有很多生物學上的相似之處幾乎是發現新藥的唯一工具,當時大多數動物都用於藥物開發。但根據歐洲的數據,如今藥物開發僅占所有動物使用量的約 20%(加上藥物安全性測試的 5% 和疫苗批次檢測的 5%);這意味著,動物使用的總量相比 1970 年代減少了大約 60%。目前,用於藥物開發的動物實驗約占動物使用總量的 30%。
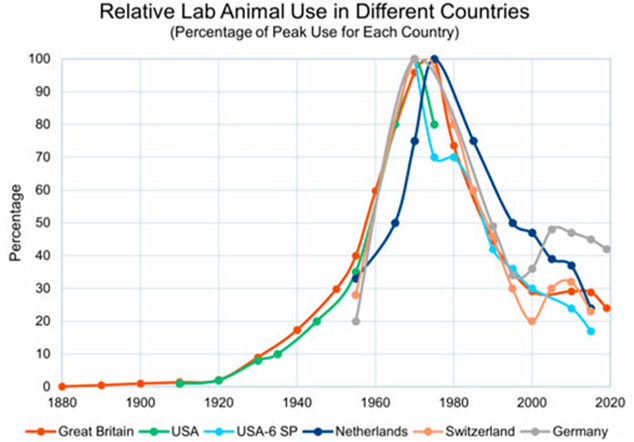
雖非使用最多,卻攸關地球生物的生死與社會貧富
另一方面,Thomas 也說到在藥物開發中,少數藥物能每年帶來數百億美元的收入,這使得藥物開發像「淘金熱」一樣,要從大量的候選藥物中篩選出少數成功者。製藥公司追求的是「重磅炸彈」藥物,年銷售額超過 10 億美元的產品,這些成功通常來自於新的疾病靶點、基因藥物或奈米顆粒等新技術,以及利用 AI 等加速開發流程的創新方法。
然而,藥物開發面臨的挑戰巨大。根據 2012 年的研究,95% 的藥物候選品在臨床階段會失敗,每個成功的藥物可能需要投入高達 26 億美元。失敗的原因通常與副作用或毒性問題相關,即使藥物成功上市,約 8% 也可能因嚴重副作用而被撤回。因此,藥物的安全性和有效性仍是上市後的重要監測重點,透過四階段臨床試驗來確保患者安全。而研發的每一款藥物,不管是失敗還是成功,都「必須」包含臨床前的動物實驗。
這個挑戰也愈發嚴峻,在醫藥產業出現了反摩爾定律 (Eroom's law),根據此定律,發展新藥物的成本,在經過通貨膨脹調整後,每隔九年就會加倍投資成本,發展風險不斷提高,新藥的創新性卻顯得又慢又長,數量也呈現非指數型成長。這是一個很大的隱憂,背後代表著花費無數的時間、人力、動物與金錢投入,重複著進行天選藥物的無效測試。

疾病舊的不去新的來得又急又快
2019 年 COVID-19 席捲全球,成為人類歷史上致死人數最多的流行病之一。COVID-19 病毒的基因序列於 2020 年 1 月公布,到同年 12 月第一個 mRNA 疫苗獲得緊急使用授權,疫苗研發僅用了不到一年,而傳統疫苗通常需要 5 到 10 年的時間。儘管疫苗如此迅速的研發出來,COVID-19 至今仍持續蔓延及變異,代表著疫苗也要跟著這些新的變異株持續研發與更新。
同時,世界上仍有許多的疾病排隊等著解藥,包括愛滋病、阿茲海默症、紅斑性狼瘡以及孤兒病等等。就算政府有因應特殊疾病推出相對應的法案,如 1983 年孤兒藥法案,旨在促進治療罕見病的藥物開發。但五花八門的疾病種類以及人類對治療藥物的需求,看起來是遠遠大於藥物開發的速度。
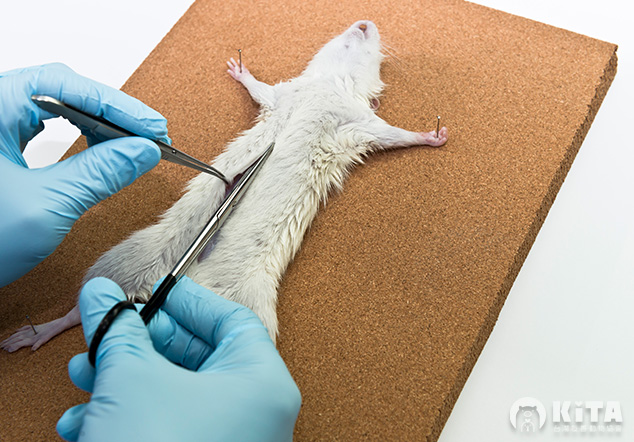
動物實驗在藥物開發上的局限性
Thomas Hartung 博士在他 2009 年發表的文章《Per aspirin ad astra》批判性地檢視了傳統動物測試方法,強調了阿斯匹靈毒理學特徵的矛盾——它能被廣泛接受是因為 1899 年缺乏嚴格的毒理學監管。作為一種廣泛使用的藥物,在動物研究中,阿斯匹靈顯示出毒性作用,如對眼睛和呼吸道的刺激、促癌作用以及胚胎畸形等,但這些在人體上並不常見或無法證實。如果在今天的嚴格監管下,阿斯匹靈可能難以通過審批。這說明了僅依賴動物實驗來預測藥物在人類的安全性是不夠的,這些差異強調了從動物實驗推測人類生理和醫學效果的局限性。近年在動物模型中引發了高度期待的 HIV 疫苗、中風治療、炎症疾病藥物以及阿茲海默症療法,在人類試驗中全部失敗。
動物實驗的模型除了有他的局限性之外,也經常無法準確預測人體臨床試驗的結果。與人體試驗的相關性僅約 37% 至 60%。這意味著動物實驗在預測藥效方面表現不佳,幾乎與隨機結果相似。即使是在不同物種之間差不多一樣的生物機制或過程,也因人與動物的差異而影響準確結果。然而,動物實驗在預測藥物安全性方面的準確性相對較高,約有 70% 的準確率能識別可能在人類中出現的毒性副作用,儘管不完美,動物測試平均來說仍較適合用於標示可能對哺乳類造成的安全問題。
過度依賴不夠充分的動物數據會導致許多潛在的好藥物被放棄或假陽性的問題發生。同時,準確度受人類和動物的生理差異、基因多樣性、測試物種的年齡健康狀況、人工誘導的疾病與自然發生的疾病變因等等因素影響。上述都一再地強調動物實驗的局限,推動科學界尋求與人類相關更好的替代方法,如「器官晶片」和先進計算模型,以提高藥物開發的準確性和安全性。

— 文 動物權特約記者 李鈺珊
______________________________
台灣友善動物協會的每項倡議都基於科學調查,專業的研究讓我們的聲音更具公信力,進而推動社會進步。為了保持調查的獨立與公正,我們拒絕來自政府和財團的捐款。協會只仰賴公眾(及少數中小企業)的小額捐助。誠邀各界支持我們,攜手為動物權益奮鬥,您的贊助是推動這場運動的重要動力。
